Тесты по химии 10 класс. Тема: "Скорость химических реакций. Химическое равновесие"
Правильный вариант ответа отмечен знаком +
1. Что способствует получению пропана в процессе химического взаимодействия С3Н6(г) + Н2(г) ↔ С3Н8(г) + Q?
- введение катализатора
+ повышение давления
- увеличение температуры
- уменьшение концентрации Н2
2. Во сколько раз целесообразно повысить давление системы, в которой происходит превращение NO в NO2, с целью повышения скорости реакции в 729 раз?
- 6
+ 9
- 8
- 12
3. Установите последовательность направленности смещения химического процесса, который описывается уравнением СО ↔ СО2 + С + Q вследствие: а) применения катализатора; б) понижения давления; в) увеличения концентрации карбона; г) возрастания температуры
- влево; влево; вправо; вправо
- влево; влево; не влияет; влево
+ не влияет; влево; не влияет; влево
- не влияет; влево; влево; вправо
4. При обычных условиях с максимальной скоростью осуществляется взаимодействие между:
- N2, О2
- Fe, S
- C2H5OH, О2
+ Na2CO3, HCl
5. Что за формула представлена на рисунке ниже?
![]()
- разности концентраций химических соединений, вступающих в химическую реакцию
+ скорости химического взаимодействия
- соотношения концентрации насыщенных и ненасыщенных растворов
- теплосодержания системы (энтальпии)
6. За счёт введения катализатора течение химического процесса ускоряется, поскольку…:
- снижается теплота реакции
- увеличивается частота соударений молекул
- повышается теплота реакции
+ снижается энергия активации
7. Как называется вещество, замедляющее процесс химической реакции?
- индикатор
- катализатор
+ ингибитор
- фермент
8. Две ёмкости заполнили равным объёмом HCl одной концентрации. В первую ёмкость добавили цинковые таблетки, во вторую - равную им по массе цинковую пыль. В какой из ёмкостей раньше завершится реакция?
- в первой
+ во второй
- в обеих одновременно
- и в том, и в другом случаях реакция протекать не будет
9. На динамическом равновесии какой из реакций не сказывается давление?
- 3Н2 + N2 ↔ 2NH3
- 2SO2 + O2 ↔ 2SO3
- CO + Cl2 ↔ COCl2
+ Н2 + Cl2 ↔ 2HCl
тест 10. Показателем необратимого химического процесса является:
- изменение цвета раствора
+ выпадение осадка
- поглощение большого количества теплоты
- все ответы верные
11. Обратимая реакция представлена уравнением:
- Na2О + 2HCl ↔ 2NaCl H2О
- FeCl3 + 3NaOH ↔ Fe(OH)3 + 3NaCl
+ N2 + 3Н2 ↔ 2NH3
- КОН + НСl ↔ KCl + Н2О
12. Химический процесс описывается уравнением А + В ↔ С + Д. Смешали по 3 моля веществ А, В, С. После установления равновесия в смеси будет находиться 4 моль вещества С. Чему будет равна константа равновесия?
- четырём
+ единице
- трём
- двум
13. С максимальной скоростью протекает:
- процесс самопроизвольного разъедания металлов на воздухе
- брожение глюкозы
+ реакция нейтрализации
- взаимодействия водорода с бромом
14. Примером обратимой химической реакции является процесс:
- растворения сахара в чае
- расширения газа в пустоту
+ гидролиза сложного эфира
- старения организма
15. Как изменяется быстрота прямой реакции С3Н8 (г) + О2 (г) = СО2(г) + Н2О(г), если в 2 раза повышается давление?
- возрастает в 128 раз
+ возрастает в 64 раза
- возрастает в 26 раз
- возрастает в 10 раз
16. Что обозначает константа скорости реакции?
- усреднённую быстроту химического процесса
+ скорость процесса при концентрации реагентов 1 моль/л
- быстроту в начальный период времени
- быстроту химического взаимодействия в определённый момент
17. Что необходимо сделать, чтобы сместить равновесие системы СО2(г) + С(тв) =2СО(г) в направлении прямой реакции?
+ понизить концентрацию СО
- увеличить давление системы
- повысить концентрацию СО
- снизить концентрацию углекислого газа
18. Между какими контактирующими веществами площадь поверхности не сказывается на скорости химического взаимодействия?
- Zn, HCl
- FeS2, O2
+ N2, H2
- CuO, Al
19. Температурный показатель реакции 2А (г) + 3В (г) = 4С (г) равен трём. Как изменится быстрота протекания реакции, если температуру снизить на 50 0С, а концентрацию реагирующих веществ повысить в три раза?
+ не изменится
- уменьшится в 243 раза
- увеличится в 243 раза
- уменьшится в 81 раз
тест-20. С понижением давления динамическому равновесию свойственно смещаться в направлении …:
- процесса, протекающего с уменьшением числа молекул продуктов реакции
- концентрации реагирующих веществ
- уменьшения количества газообразных веществ
+ увеличения объёма реакционной смеси
21. В каком направлении и как изменится равновесие системы СО ↔ СО2 + С + Q с увеличением давления и снижением температуры соответственно?
- не изменится; вправо
+ вправо; вправо
- влево; влево
- вправо, влево
22. Катализатор AlCl3 увеличивает быстроту:
- любого химического взаимодействия между органическими соединениями
+ некоторых химических процессов между органическими веществами
- любого взаимодействия между неорганическими соединениями
- некоторых реакций между неорганическими веществами
23. Выберите верное значение: «Длительность химической реакции с температурным коэффициентом 2 (значение коэффициента равно для 30 0С) заканчивается через 5 мин. Чтобы ускорить протекание данной реакции до 30 с, следует повысить температуру на … градусов Цельсия».
+ 130
- 100
- 50
- 300
24. От какого показателя не зависит скорость химического взаимодействия в растворах?
- объёма реакционной посуды
- катализатора
- концентрации веществ
+ индикатора
25. В какой из систем произойдёт одностороннее изменение химического равновесия, если в ней повысить давление и снизить температуру?
- С2H2(г)↔ 2С + Н2 - Q
+ N2 + 3Н2 ↔2NH3 + Q
- N2 + О2↔ 2NO - Q
- Н2 + Cl2↔ 2HC1 + Q
26. Как отражается на поведении реакции повышение температуры?
- никак не сказывается на её скорости
+ возрастает быстрота реакции
- снижается скорость реакции
- нет верного ответа
27. Для изменения равновесия химического взаимодействия согласно уравнению CaCO3(т) = CaO(т) + CO2(т) - Q в направлении продуктов реакции следует:
+ увеличить Т
- снизить Т
- увеличить р
- ввести в систему катализатор
28. Какие факторы (а) увеличение концентрации азота, б) температура, в) давление, г) уменьшение концентрации кислорода, д) катализатор) не влияют на равновесие химического процесса N2 (г) + O2 (г) ↔ NO (г) - 180, 7 кДж/моль?
- 1, 2, 4
- 2, 3
+ 3, 5
- 1, 2
29. Укажите, что за формула представлена на рисунке ниже:
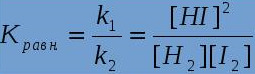
- расчёта концентрации веществ химического взаимодействия
- определения константы растворимости
+ вычисления константы химического равновесия
- определения константы диссоциации слабых электролитов
тест_30. Насколько справедливы представленные ниже утверждения относительно смещения химического равновесия системы 2CO(г) + O2(г) = 2CO2(г) + Q?
1. Со снижением давления произойдёт смещение химического равновесия системы в направлении продукта реакции.
2. С увеличением концентрации СО2 наблюдается смещение химического равновесия системы в сторону продукта реакции.
- справедливо лишь утверждение 1
- справедливо лишь утверждение 2
- справедливы оба утверждения
+ оба утверждения неверны
