Тесты по химии 8 класс. Тема: "Химические связи. Кристаллические решетки"
Правильный вариант ответа отмечен знаком +
1. Какую разновидность кристаллической решетки имеют щелочи?
- атомную
- молекулярную
+ ионную
- металлическую
2. Укажите общее число совместных электронных пар в молекуле азота:
- 2
+ 3
- 1
- 4
3. Узлы кристаллической решетки Cu содержат:
- молекулы
- атомы
+ атомы и ионы
- ионы
4. Укажите вещество с металлическим типом кристаллической решетки:
+ Al
- С (графит)
- O2
- B
5. Как называется химически неделимая, не претерпевающая распада, структурная часть любого соединения (см. рис.)?
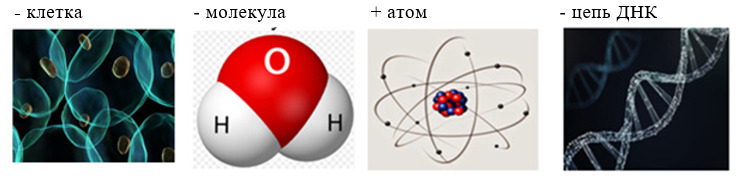
6. Белый фосфор имеет тип химической связи:
- двойную ионную
- тройную ковалентную полярную
- металлическую
+ одинарную ковалентную неполярную
7. Как называется собственный момент импульса элементарной частицы?
+ спин
- инертность
- облако
- валентность
8. Для ковалентной разновидности связи характерна:
- высокая температура плавления
- ненаправленность
- ненасыщаемость
+ полярность
9. Укажите разновидность кристаллической решетки, характерную для оснований и солей:
- металлическая
+ ионная
- молекулярная
- атомная
тест 10. Укажите вещество с ковалентной полярной связью:
- кислород
+ йодоводород
- хлор
- бромид натрия
11. Как называются отрицательно заряженные ионы?
- электроны
- нейтроны
+ анионы
- катионы
12. Металлическая разновидность химической связи формируется между атомами:
- мышьяка
+ цезия
- водорода
- азота
13. Укажите простой ион:
+ Cl-
- CO32-
- OH-
- NH4+
14. Обозначьте правильный ответ «В молекуле SO3 …»:
- сера образовывает 4 одинаковые одинарные взаимосвязи
- электронная плотность связи «сера-кислород» смещена в сторону серы
- между атомами S и O формируется ковалентный неполярный тип связи
+ имеется между атомами двойная взаимосвязь
15. Не относится к парамагнетикам:

16. Металлическая связь формируется за счет … электронов.
- свободных
- внешних
- полярных
+ валентных
17. Тип химической связи «ковалентная полярная» наиболее выражен у:
+ воды
- тетрахлорметана
- фторида лития
- хлорида натрия
18. Укажите, какой характер взаимодействия между частицами, расположенными в узлах кристаллической решетки, характерный для металлического типа кристаллической решетки:
- ионная связь
- ковалентная связь
+ металлическая связь
- силы межмолекулярного взаимодействия
19. Закончите предложение: «Правильное расположение микроскопических частиц вещества в кристалле называется кристаллическая…».
- схема
+ решетка
- матрица
- модель
тест-20. Укажите неполярную молекулу:
- CO2
- NH3
+ BF3
- CCl4
21. Какой вид агрегатного состояния присущ химическим соединениям с ионным типом кристаллической решетки?
- жидкое
- газообразное
+ твердое
- все ответы верные
22. Укажите основное свойство веществ с атомным типом кристаллической решетки:
- быстрая электропроводность
- легкоплавкость
- хрупкость
+ высокая твердость и тугоплавкость
23. Насколько прочными являются связи в соединениях с молекулярным типом кристаллической решетки?
- весьма прочными
- совсем непрочными
+ слабо прочными
- им может быть свойственна разная прочность
24. Укажите соединение с ионным типом кристаллической решетки:
- O3
- твердый CO2 («сухой лед»)
- SiO
+ Al2(SO4)3
25. Возможность атома образовывать некое количество химических связей называется:
+ валентность
- частотность
- инертность
- пассивность
26. Какой тип кристаллической решетки имеют белый фосфор и глюкоза?
- ионную
- атомную
+ молекулярную
- металлическую
27. Самая высокая температура плавления характерна для:
+ C (графит)
- HF
- NaCl
- O2
28. Кристаллическое строение имеет:
- смола
+ пищевая соль
- воск
- все выше перечисленные вещества
29. Пластичность характерна для химических соединений с … типом кристаллической решетки.
- ионным
- молекулярным
+ металлическим
- атомным
тест_30. Ковалентная полярная связь может образовываться между атомами:
+ всех неметаллов с разной электроотрицательностью
- всех неметаллов и металлов
- любых неметаллов с одинаковым значением электроотрицательности
- только металлов с одинаковым показателем отрицательности
