Примеры решения тестовых заданий по Химии
Решение и правильный ответ даны после каждого задания.
Задание 1. В воде массой 100 г растворили хлорид натрия массой 10 г. Чему равна массовая доля полученного раствора?
1. 0,1
2. 11 %
3. 10 %
4. 9 %
5. 0,9
Решение:
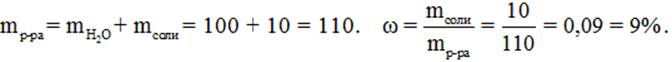
Правильный ответ - четвёртый.
Задание 2. Определите массу гидроксида натрия в 100 л раствора с молярной концентрацией 0,1 моль/л.
1. 10 кг
2. 400 г
3. 40 кг
4. 10 г
5. 40 г
Решение:
Из формулы молярной концентрации: 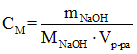 следует, что mсоли = CM
следует, что mсоли = CM![]() Mсоли
Mсоли![]() Vр-ра.
Vр-ра.
По периодической таблице MNaOH = 23 + 16 + 1 = 40 г/моль.
mсоли = 0,1![]() 40
40![]() 100 = 400 г.
100 = 400 г.
Правильный ответ – второй.
Задание 3. В 100 л раствора (r = 1 г/мл) содержится гидроксид кальция массой 100 г. Определите величину эквивалентной концентрации (нормальность) раствора (экв/л).
1. 0,027
2. 0,014
3. 1
4. 0,1
5. 74
Решение: формула эквивалентной концентрации: 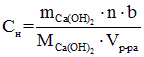 , где n = 1 (один атом металла в молекуле), b = 2 (величина заряда металла Ca+2).
, где n = 1 (один атом металла в молекуле), b = 2 (величина заряда металла Ca+2).
Определим молярную массу ![]() 40 + 2(16 + 1) = 74 г/моль.
40 + 2(16 + 1) = 74 г/моль.
Рассчитываем: ![]() = 0,027 экв/л.
= 0,027 экв/л.
Правильный ответ – первый.
Задание 4. Определите объём (мл) воды, которую надо добавить к 50 %-ному раствору хлорида натрия массой 100 г, чтобы получить 20 %-ный раствор.
1. 500
2. 200
3. 250
4. 150
5. 158
Решение: из формулы массовой доли:mсоли = w![]() mр-ра = 0,5
mр-ра = 0,5![]() 100 = 50 г.
100 = 50 г.
При добавлении воды масса соли не изменится, поэтому 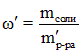 и
и 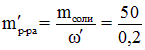 = 250 г. Но это ещё не ответ, т. к.
= 250 г. Но это ещё не ответ, т. к. ![]() , то есть добавить к 100 г исходного раствора надо 150 г воды. Плотность воды – 1 г/мл, поэтому правильный ответ – четвёртый.
, то есть добавить к 100 г исходного раствора надо 150 г воды. Плотность воды – 1 г/мл, поэтому правильный ответ – четвёртый.
Задание 5. Смешали 5 л 1М раствора с 1 л 5М раствора гидроксида натрия. Определите молярную концентрацию образовавшегося раствора (моль/л).
1. 1
2. 1,7
3. 1,2
4. 1,5
5. 2
Решение: 1М и 5М – обозначения молярных концентраций 1 моль/л и 5 моль/л соответственно.
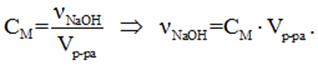
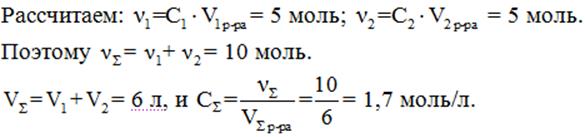
Правильный ответ – второй.
Задание 6. В воде содержатся гидрокарбонат натрия и хлорид кальция. После растворения в ней карбоната натрия:
1. общая жёсткость не изменится
2. общая жёсткость уменьшится
3. временная жёсткость уменьшится
4. временная жёсткость не изменится
5. постоянная жёсткость уменьшится
Решение: карбонат натрия – основной компонент соды – вещества, используемого для полного устранения жёсткости, поэтому при его растворении в воде снижаются все виды жёсткости: и временная, и постоянная, и общая.
Правильные ответы – второй, третий и пятый.
Задание 7. В воде содержатся катионы и анионы в следующих концентрациях: (мэкв/л): Ca2+ – 1,8; Na+ – 3,0; Mg2+ – 0,9; HCO3- – 3,8; SO42- – 0,8; Cl- – 1,1. Определите величину общей жёсткости этой воды (мэкв/л).
1. 1,8
2. 2,7
3. 5,8
4. 1,9
5. 5,7
Решение: Общую жёсткость придают воде только катионы металлов: Ca2+, Mg2+, Fe2+ иMn2+. Другие ионы жёсткости не дают.
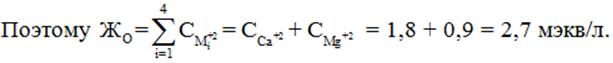
Правильный ответ – второй.
